A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Fosfán | |||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||||||||
| Sumárny vzorec | PH3 | ||||||||||||||||||||||||||||||||||||||||
| Systematický názov | Fosfán | ||||||||||||||||||||||||||||||||||||||||
| Synonymá | Fosfín | ||||||||||||||||||||||||||||||||||||||||
| Vzhľad | Bezfarebná plynná látka | ||||||||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 34,0 u | ||||||||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 33,998 g/mol | ||||||||||||||||||||||||||||||||||||||||
| Rozpustnosť vo vode | 33 mg/100 ml (20 °C) | ||||||||||||||||||||||||||||||||||||||||
| Teplota topenia | -133,5 °C | ||||||||||||||||||||||||||||||||||||||||
| Teplota varu | -87,43 °C | ||||||||||||||||||||||||||||||||||||||||
| Kritická teplota | 51,3 °C | ||||||||||||||||||||||||||||||||||||||||
| Kritický tlak | 6 510 kPa | ||||||||||||||||||||||||||||||||||||||||
| Hustota | 0,001529 g/cm3 (0 °C) 0,746 g/cm3 (-90 °C) 0,896 g/cm3 (-135 °C) | ||||||||||||||||||||||||||||||||||||||||
| Rozpustnosť | v polárnych rozpúšťadlách: etanol dietyléter v nepolárnych rozpúšťadlách: aromatické uhľovodíky | ||||||||||||||||||||||||||||||||||||||||
| Teplota vzplanutia | 38 °C | ||||||||||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||||||||||
| Entropia topenia | 33,2 J/g | ||||||||||||||||||||||||||||||||||||||||
| Entropia varu | 429,7 J/g | ||||||||||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | 9,25 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Štandardná entropia | 210,2 J K-1 mol-1 | ||||||||||||||||||||||||||||||||||||||||
| Štandardná Gibbsová energia | 13,4 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 1,091 J K-1 g-1 | ||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||||||||
| Číslo CAS | 7803-51-2 | ||||||||||||||||||||||||||||||||||||||||
| Číslo UN | 2199 | ||||||||||||||||||||||||||||||||||||||||
| EINECS číslo | 232-260-8 | ||||||||||||||||||||||||||||||||||||||||
| Číslo RTECS | SY7525000 | ||||||||||||||||||||||||||||||||||||||||
| PubChem | 24404 | ||||||||||||||||||||||||||||||||||||||||
| ChemSpider | 22814 | ||||||||||||||||||||||||||||||||||||||||
| SMILES | P | ||||||||||||||||||||||||||||||||||||||||
| 3D model (JSmol) | Interaktívny 3D model | ||||||||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||||||||

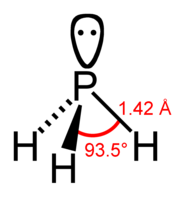
Fosfán (PH3) je hydrid fosforu. Molekula má tvar pyramídy s uhlom HPH = 93,5°. Čistý fosfán nie je samovznietivý ale v prítomnosti stôp difosfánu, P2H4, alebo pár bieleho fosforu, P4, sa vznecuje. Zapálený sa oxiduje vzduchom a môže tvoriť explózivné zmesi. Je veľmi jedovatý.
Chemické vlastnosti
Na rozdiel od amoniaku, NH3, nie je v kvapalnom stave asociovaný a je len nepatrne rozpustný vo vode. Roztoky nie sú ani kyslé ani zásadité. Reaguje však s niektorými kyselinami za vzniku fosfoniových solí:
Fosfán je tiež silným redukčným činidlom a reaguje s roztokmi mnohých kovových iónov za vzniku fosfidov. V zásaditom roztoku prebieha reakcia:
- .
Čistý plyn je bez zápachu, typický zápach technického fosfánu po rybine alebo cesnaku je spôsobený nečistotami.[1]
Toxicita
Hlavná vstupná cesta do organizmu je vdychovanie plynného fosfánu. Pri požití kovových fosfidov (najmä hliníka a zinku) dochádza v tráviacom trakte k hydrolýze a uvoľneniu fosfánu. Vdychovanie plynu spôsobuje silné podráždenie pľúc, ich edém, srdcovú dysfunkciu, excitáciu CNS, kómu, prípadne smrť. Objavujú sa tiež zažívacie ťažkosti, poškodenie obličiek a leukopénia.[1]
Po požití fosfidov sa objavuje podráždenie vedúce až ku krvácaniu, obehový kolaps, neuropsychiatrické problémy, zlyhanie dýchacích funkcií a obličiek. Neskôr sa môže objaviť poškodenie pečene. Bol publikovaný rad správ o vysokej mortalite (nad 50%) u otráv fosfidmi v Indii.[1] Fosfid zinku sa skôr používal ako rodenticíd.
K smrti pri otrave dochádza obvykle do štyroch dní, ale môže k nej dôjsť za jeden alebo dva týždne. Posmrtné analýzy ukázali infiltráciu a nekrózu srdcového svalu, pľúcny edém a poškodenie malých ciev.[1]
Chronická expozícia spôsobuje bolesti zubov, opuch až nekrózu čeľuste, slabosť, stratu váhy, anémiu a samovoľné zlomeniny.[1]
Fosfán sa z tela vylučuje jednak nezmenený vo vydychovanom vzduchu, a ďalej tiež močom v podobe fosfornanov a fosforitanov. Oxidácia fosfánu v tele je pomalá. Denaturuje oxyhemoglobín a inhibuje radu enzýmov.[1]
Boli zaznamenané prípady smrteľných otráv už pri koncentrácii fosfánu 1,2mg/m³. Pri požití fosfidu zinku nastala smrť už pri dávke 4,5g, naopak bolo hlásených prežitie i u dávky 50g.[1]
U králikov sa pri koncentrácii 70 mg/m³ po dobu 10 minút neobjavili žiadne príznaky, ale expozícia koncentrácii 140 mg/m³ bola smrteľná počas 2,5 – 3 hodín a pri koncentrácii 700 mg/m³ nastala smrť za 25 – 30 minút. Pri podávaní fosfidu zinku potkanom uhynulo 1 z 12 zvierat pri 200 mg/kg a pri 500 mg/kg 10 z 12 zvierat. Dávka 100 mg/kg a menej nebola smrteľná, ale bol pozorovaný úbytok hemoglobínu a červených krviniek.[1]
Referencie
Literatúra
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabuľky. 1. vyd. Praha : Grada Publishing, 1999. ISBN 80-7169-855-5.
Pozri aj
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Fosfan na českej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk














