A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Fosforečnan | |
 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | PO43- |
| Synonymá | ortofosforečnan |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 94,973 g/mol |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
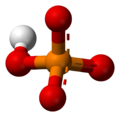
Fosforečnan alebo fosfát je soľ kyseliny fosforečnej. Fosforečnanový anión má empirický vzorec PO43−.
V roztoku dochádza v závislosti od pH k protonizácii fosforečnanového aniónu, takže sa môže vyskytovať ako
- fosforečnan PO43−
- hydrogénfosforečnan HPO42−
- dihydrogénfosforečnan H2PO4−
-
H3PO4
kyselina fosforečná -
H2PO4−
dihydrogénfosforečnanový anión -
HPO42−
hydrogénfosforečnanový anión -
PO43−
fosforečnanový anión
Chemické vlastnosti
Fosforečnanový ión má fosforový atóm obklopený štyrmi atómami kyslíka v tetraédrickom usporiadaní. Fosforečnanový ión je konjugovanou bázou hydrogénfosforečnanového iónu HPO42-, ktorý je zase konjugovanou bázou dihydrogénfosforečnanového iónu H2PO4-, ktorý je konjugovanou bázou kyseliny ortofosforečnej, H3PO4.
Mnoho fosforečnanov je pri štandardnej teplote a tlaku rozpustných vo vode. Fosforečnany sodný, draselný, rubídny, cézny a amónny sú všetky rozpustné vo vode. Väčšina ostatných fosforečnanov je vo vode len málo rozpustná alebo úplne nerozpustná. Vo všeobecnosti sú hydrogénfosforečnan a dihydrogénfosforečnan o niečo lepšie rozpustné, než odpovedajúce fosforečnany.
Rovnováha v roztoku

Vo vodnom roztoku existuje kyselina fosforečná a jej tri anióny v rovnováhe, ktorá je daná disociačnými konštantami:[1]
| Rovnováha | Disociačná konštanta Ka[2] | pKa |
|---|---|---|
| H3PO4 ⇌ H2PO4- + H+ | Ka1 = / ≈ 7.5 × 10−3 | pKa1 = 2.14 |
| H2PO4- ⇌ HPO42- + H+ | Ka2 = / ≈ 6.2 × 10−8 | pKa2 = 7.20 |
| HPO42- ⇌ PO43− + H+ | Ka3 = / ≈ 2.14 × 10−13 | pKa3 = 12.37 |
Hodnoty sú udané pre 25 °C a iónovú silu I = 0.
pKa hodnoty odpovedajú pH, pri ktorom je v roztoku koncentrácia zlúčeniny zhodná s jej konjugovanou bázou. Pri pH nižšom než 1 je kyselina fosforečná prakticky úplne nedisociovaná. Okolo pH 4,7 (v strede medzi prvými dvoma pKa) je prakticky jedinou prítomnou formou v roztoku. Pri pH okolo 9,8 (v strede medzi druhými dvoma pKa) je hlavnou formou HPO42-. Pri pH nad 13 existuje kyselina fosforečná ako úplne disociovaný fosforečnanový anión, PO43−.
Vďaka tomu je možné kryštalizovať soli hydrogénfosforečnanov a dihydrogénfosforečnanov nastavením pH, konkrétne pri 4,7 a 9,8.
Fosforečnanové anióny, H2PO4-, HPO42- a PO43−, sa chovajú ako samostatné slabé kyseliny, pretože ich pKa sa líši o viac ako 4.
Fosforečnany tvoria i polymérne ióny, napríklad pyrofosfát (P2O7)4- alebo trifosfát (P3O10)5-. Rôzne metafosfátové ióny (zvyčajne ako lineárne polyméry) majú empirický vzorec (PO3)- a sú prítomné v mnohých zlúčeninách.
Biochémia fosfátov
V biologických systémoch sa fosfor často nachádza vo forme voľných fosfátových iónov, kde sa zvyčajne nazýva anorganický fosfát, alebo viazaný na organické molekuly v podobe organofosfátov.
Anorganický fosfát sa v biochémii často zapisuje ako Pi a pri fyziologickom pH pozosáva hlavne z iónov HPO42- a H2PO4-. Pri neutrálnom pH, napríklad v cytozole (pH = 7), je pomer koncentrácií približne:
- / ≈ 7.5 × 104
- / ≈ 0.62
- / ≈ 2.14 × 10−6
Na základe toho sú prítomné v cytozole vo významnom množstve len HPO42- a H2PO4- (38 % HPO42- a 62 % H2PO4-). V extracelulárnej tekutine (pH = 7,4) je tento pomer opačný (61 % HPO42- a 39 % H2PO4-).
Anorganický fosfát môže byť prítomný i v podobe pyrofosfátu, ktorý hydrolýzou dáva ortofosfát:
- 4- + H2O ⇌ 2 2-
Organické fosfáty sa častejšie nachádzajú v podobe esterov ako nukleotidy (napr. AMP, ADP a ATP) a v DNA a RNA. Voľný ortofosfátový anión sa uvoľňuje hydrolýzou fosfoanhydridovej väzby v ADP alebo ATP. Tieto fosforylačné a defosforylačné reakcie sú skladiskom a zdrojom chemickej energie pre mnoho metabolických procesov. ATP a ADP sa občas označujú ako vysokoenergetické fosfáty, podobne i fosfagény v svaloch. Podobné reakcie existujú i pre difosfáty a trifosfáty ostatných nukleozidov.
Kosti a zuby
Dôležitou úlohou fosfátu v biologických systémoch je ich použitie ako štruktúrny materiál v kostiach a zuboch. Tieto štruktúry sa skladajú z fosforečnanu vápenatého vo forme hydroxyapatitu. Tvrdá zubná sklovina cicavčích zubov je tvorená fluoroapatitom, fosforečnanom hydroxyvápenatým, kde sú niektoré hydroxylové skupiny nahradené fluoridovými aniónmi.
Referencie
- ↑ CAMPBELL, Neil A.; Reece, Jane B.. Biology. Seventh. vyd. San Francisco, California : Benjamin Cummings, 2005. ISBN 0-8053-7171-0. S. 65.
- ↑ Kipton J. Powell, Paul L. Brown, Robert H. Byrne, Tamás Gajda, Glenn Hefter, Staffan Sjöberg, Hans Wanner (2005): "Chemical speciation of environmentally significant heavy metals with inorganic ligands. Part 1: The Hg2+, Cl−, OH−, CO32−, SO42−, and PO43− aqueous systems". Pure and Applied Chemistry, volume 77, issue 4, pages 739–800. DOI:10.1351/pac200577040739
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Phosphate na anglickej Wikipédii.
Externé odkazy
- FILIT – zdroj, z ktorého pôvodne čerpal tento článok.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk