A | B | C | D | E | F | G | H | CH | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9
| Chlorid meďný | |||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||
| Sumárny vzorec | CuCl | ||||||||||||||||||||||||||||||||
| Vzhľad | biely prášok | ||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 99,0 u | ||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 98,999 g/mol | ||||||||||||||||||||||||||||||||
| Teplota topenia | 430 °C | ||||||||||||||||||||||||||||||||
| Teplota varu | 1 212 °C | ||||||||||||||||||||||||||||||||
| Hustota | 4,139 g/cm³ | ||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: 1,25 g/100 ml v polárnych rozpúšťadlách: kyselina chlorovodíková roztoky amónnych solí roztoky kyanidov | ||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||
| Entropia topenia | 103,5 J/g | ||||||||||||||||||||||||||||||||
| Entropia varu | 219,2 J/g | ||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | −136,5 kJ/mol | ||||||||||||||||||||||||||||||||
| Štandardná entropia | 87,1 J K−1 mol−1 | ||||||||||||||||||||||||||||||||
| Štandardná Gibbsová energia | −114,06 kJ/mol | ||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 0,489 9 J K−1 g−1 | ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||
| Číslo CAS | 7758-89-6 | ||||||||||||||||||||||||||||||||
| Číslo UN | 2802 | ||||||||||||||||||||||||||||||||
| EINECS číslo | 231-842-9 | ||||||||||||||||||||||||||||||||
| Číslo RTECS | GL6990000 | ||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||
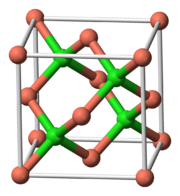
Chlorid meďný (CuCl) je anorganická zlúčenina, jeden z chloridov medi. Ide o bielu tuhú látku zle rozpustnú vo vode, ale dobre rozpustnú v koncentrovanej kyseline chlorovodíkovej. Nečisté vzorky sú zelenkasté vďaka prítomnosti zeleného chloridu meďnatého.[1]
Vlastnosti

Chlorid meďný je Lewisova kyselina, klasifikovaná podľa konceptu HSAB ako „mäkká“. Preto má tendenciu tvoriť stabilné komplexy s mäkkými Lewisovými hydroxidmi, napríklad trifenylfosfínom:
- CuCl + P(C6H5)3 → 4
Hoci sa chlorid meďný príliš nerozpúšťa vo vode, rozpúšťa sa vo vodných roztokoch obsahujúcich vhodné donorové molekuly. Tvorí komplexy s halogenidovými iónmi; napríklad s koncentrovanou kyselinou chlorovodíkovou tvorí H3O+CuCl2-. Podobne tvorí komplexy aj s aniónom kyanidu, aniónom tiosíranu a amoniakom.
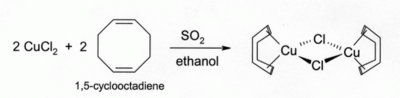
Roztoky chloridu meďného s chlorovodíkom alebo amoniakom pohlcujú oxid uhoľnatý za vzniku bezfarebných komplexov, napríklad diméru s chloridovým mostíkom 2. Rovnaký roztok s chlorovodíkom reaguje tiež s acetylénom na . Roztok s amoniakom dáva s acetylénom výbušný acetylid meďný. Komplexy chloridu meďného s alkénmi možno pripraviť redukciou chloridu meďnatého oxidom siričitým za prítomnosti alkénu v alkoholovom roztoku. Komplexy s diénmi, napr. 1,5-cyklooktadiénom, sú obzvlášť stabilné:[2]
Za neprítomnosti iných ligandov sú vodné roztoky chlorid meďného nestabilné vzhľadom k disproporcionácii na meď a chlorid meďnatý.[3] Čiastočne z tohto dôvodu sa chlorid meďný na vzduchu sfarbuje dozelena.
Použitie
Hlavné použitie chloridu meďného je ako prekurzor pre výrobu fungicídneho oxychloridu meďnatého. Na tento účel sa chlorid meďný generuje synproporcionáciu a potom sa oxiduje vzduchom:
- Cu + CuCl2 → 2 CuCl
- 6 CuCl + 3/2 O2 + 3 H2O → 2 Cu3Cl2(OH)4 + CuCl2
Chlorid meďný katalyzuje veľa organických reakcií. Jeho afinita k oxidu uhoľnatému v prítomnosti chloridu hlinitého sa využíva v procese COPureSM.
Organická syntéza
V Sandmeyerovej reakcii vedie pôsobenie chloridu meďného na aréndiazóniové soli k vzniku arylchloridov, napríklad:[4]

Táto reakcia má široký záber a obvykle ponúka vysokú výťažnosť.
Polyméry
Chlorid meďný sa používa ako katalyzátor v radikálovej polymerizácii prenosom atómu (ATRP).
Podobné zlúčeniny
Referencie
- ↑ United States Patent US4582579 "method of preparing cupric ion free cuprous chloride" Section 2, lines 4-41, via www.freepatentsonline.com
- ↑ Nicholls, D. Complexes and First-Row Transition Elements, Macmillan Press, London, 1973.
- ↑ Greenwood, N.N.; Earnshaw, A. Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997.
- ↑ (a) Wade, L. G. Organic Chemistry, 5th ed., p. 871, Prentice Hall, Upper Saddle RIver, New Jersey, 2003. (b) March, J. Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992.
Iné projekty
 Commons ponúka multimediálne súbory na tému Chlorid meďný
Commons ponúka multimediálne súbory na tému Chlorid meďný
Literatúra
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabuľky. 1. vyd. Praha : Grada Publishing, 1999. ISBN 80-7169-855-5.
- Mellor, J. W., A Comprehensive Treatise on Inorganic and Theoretical Chemistry, Volume III, pp157-168. Longmans, Green & Co., London, 1967 (new impression)
Externé odkazy
- National Pollutant Inventory - Copper and compounds fact sheet
- The COPureSM Process for Purifying CO utilizing a copper chloride complex
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Chlorid měďný na českej Wikipédii.
Text je dostupný za podmienok Creative Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších podmienok. Podrobnejšie informácie nájdete na stránke Podmienky použitia.
Antény
Chemické zdroje elektriny
Chladenie v elektrotechnike
Elektrická sústava automobilu
Elektrická trakcia
Elektrické prístroje
Elektrické súčiastky
Elektrické spotrebiče
Elektrické stroje
Čítanie (elektrotechnika)
Činný výkon
Štatistická dynamika
Živý vodič
Admitancia
Antiparalelné zapojenie
Asynchrónny motor
Blúdivý prúd
Bočník (elektrotechnika)
Diak (polovodičový prvok)
Displej s kvapalnými kryštálmi
Elektrická inštalácia
Elektrická rezonancia
Elektrická sila
Elektrická vodivosť
Elektrické zariadenie
Elektrický obvod
Elektrický zvonec
Elektroenergetika
Elektromer
Elektrometer
Elektromobil
Elektromotor
Elektromotorické napätie
Elektrotechnický náučný slovník
Elektrotechnika
Elektrotechnológia
Fázor
Faradayova klietka
Frekvencia (fyzika)
Graetzov mostík
Impedancia
Indukčnosť
Induktancia
Istič
Izolácia (elektrotechnika)
Izolant
Jadro vodiča
Jednobran
Jednosmerný prúd
Joulovo teplo
Katóda
Koaxiálny kábel
Kompenzácia účinníka
Konduktometria
Konektor (elektrotechnika)
Korónový výboj
Lanko (elektrotechnika)
Leptanie
Logické hradlo
Magnetická susceptibilita
Magnetizácia (veličina)
Merný elektrický odpor
Mobilné zariadenie
Napájací zdroj
Napäťový chránič
Napäťový násobič
Nortonova veta
Odpínač
Odpojovač
OLED
Olovený akumulátor
Paralelné zapojenie
Peltierov článok
Plošná hustota elektrického prúdu
Poistka (elektrotechnika)
Posuvný prúd
Prúdový chránič
Prenosové médium
Prieletový klystrón
Primárny elektrochemický článok
Reaktancia
Rekuperácia (dopravný prostriedok)
Relé
Reproduktorová výhybka
Rezistancia
Rozhranie (interface)
Sériové zapojenie
Seebeckov jav
Sekundárny elektrochemický článok
Settopbox
Skrat
Sonar
Spínač
Spínaný zdroj
Straty v mikropásikových vedeniach
Striedavý prúd
Stupeň ochrany krytom
Svetelná výbojka
Symetrizačný člen
Technická normalizácia
Tepelné relé
Tepelne vodivostný detektor
Termočlánok
Théveninova veta
Transformátor
Transformátor s fázovou reguláciou
Trojfázová sústava
Tuhá fáza (elektronika)
Tyratrón
Usmerňovač (elektrotechnika)
Uzemnenie
Uzol (vodiče)
Vírivý prúd
Výbojka
Varistor
Ventilátor
Vodič (elektrotechnika)
Voltov stĺp
Vstavaný systém
Zásuvka (elektrotechnika)
Zdroj (elektrotechnika)
Zisk antény
Text je dostupný za podmienok Creative
Commons Attribution/Share-Alike License 3.0 Unported; prípadne za ďalších
podmienok.
Podrobnejšie informácie nájdete na stránke Podmienky
použitia.
www.astronomia.sk | www.biologia.sk | www.botanika.sk | www.dejiny.sk | www.economy.sk | www.elektrotechnika.sk | www.estetika.sk | www.farmakologia.sk | www.filozofia.sk | Fyzika | www.futurologia.sk | www.genetika.sk | www.chemia.sk | www.lingvistika.sk | www.politologia.sk | www.psychologia.sk | www.sexuologia.sk | www.sociologia.sk | www.veda.sk I www.zoologia.sk







